SARS-COV-2 et syndrome de détresse respiratoire aiguë (SDRA)
Par Maylis Dagouassat et Danushki Herath
Le coronavirus SARS-CoV-2 a été identifié en Chine en décembre 2019. La maladie provoquée par ce coronavirus a été nommée COVID-19 par l’organisation mondiale de la santé (OMS). Les formes graves de COVID-19 touchent majoritairement les personnes âgées et celles fragilisées par d’autres maladies (diabète, asthme, problèmes pulmonaires, cardiaques ou rénaux…). Les symptômes les plus fréquents sont de la fièvre, de la toux, une gêne respiratoire pouvant aller jusqu’au syndrome de détresse respiratoire aiguë (SDRA). Ce syndrome survient lors d’une diminution des apports en dioxygène aux organes. Ceci est dû à une incapacité des poumons à fonctionner correctement. C’est une urgence vitale qui peut conduire à la mort.
1. Comment le virus déclenche-t-il un syndrome de détresse respiratoire aiguë ?
Le coronavirus entre dans l’organisme par le nez, la bouche ou les yeux. Il va ensuite passer par la trachée, les bronches, les bronchioles pour atteindre les alvéoles pulmonaires (figure 1). Les alvéoles sont des petits sacs situés à l’extrémité des bronchioles qui assurent les échanges gazeux. Ces alvéoles sont entourés de vaisseaux sanguins dans lesquels les globules rouges libèrent du dioxyde de carbone (CO2) et récupèrent du dioxygène (O2). Les cellules qui composent les alvéoles sont appelées pneumocytes. Les échanges gazeux s’effectuent au niveau des pneumocytes de type I. Les pneumocytes de type II produisent le surfactant qui maintient la forme de l’alvéole.

Illustration issue d’Avessa Roston et traduit par Richard Ying (KezaCovid19 (@Kezacovid)
Au niveau des alvéoles, le virus infecte les pneumocytes de type II. En effet le virus va chercher une « clef » afin d’entrer dans ces cellules. Cette clé est présente à la surface des pneumocytes c’est un récepteur appelé ACE2. Le virus va se fixer sur ACE2 grâce aux protéines appelées spicules qui le recouvrent (figure 2). Une fois, à l’intérieur le virus va injecter son ARN dont l’expression va obliger la cellule infectée à produire de nouveaux virus. La cellule hôte est ensuite détruite et les nouveaux virus libérés dans les alvéoles vont aller infecter d’autres cellules.
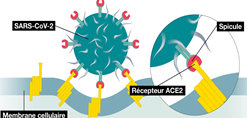
L’entrée du virus dans les pneumocytes de type II va déclencher une réaction inflammatoire. Les pneumocytes vont envoyer des signaux qui vont activer les macrophages. Ces cellules sont capables d’ingérer et de détruire des bactéries ou des microbes. Ces macrophages vont libérer des substances nommées cytokines (IL-6, IL-2…) (protéines du système immunitaire) qui vont attirer d’autres globules blancs sur le site de l’infection et vont dilater les vaisseaux sanguins pour faciliter leur passage. Ceci s’accompagne d’une entrée de liquide plasmatique du sang (composant liquide du sang) vers les alvéoles. L’œdème pulmonaire formé par cette fuite de liquide va diluer le surfactant et fragiliser les alvéoles. Les neutrophiles (globules blancs) vont détruire les pneumocytes infectés par le virus ce qui va conduire à un affaissement des alvéoles (sur elles-mêmes) et à l’apparition du syndrome de détresse respiratoire (SDRA, figure 3). Les cytokines jouent un rôle très important dans le syndrome respiratoire aiguë. Leur libération par les macrophages et les globules blancs devient incontrôlée et on parle alors d’une « tempête cytokinique ». Cette dernière va participer à la destruction des pneumocytes et à la diminution des apports en dioxygène. En parallèle, des cellules présentes sur le lieu de l’infection nommée cellules dendritiques vont se diriger vers les ganglions lymphatiques. Ces cellules vont activer les lymphocytes T spécifiques du virus quelques jours après son entrée. Ces lymphocytes vont ensuite se diriger vers les alvéoles pulmonaires et vont participer à la destruction des cellules infectées par le coronavirus. Cependant, dans le SDRA, ces lymphocytes sont diminués, ce qui favorise la réplication de virus et sa dispersion dans les poumons.
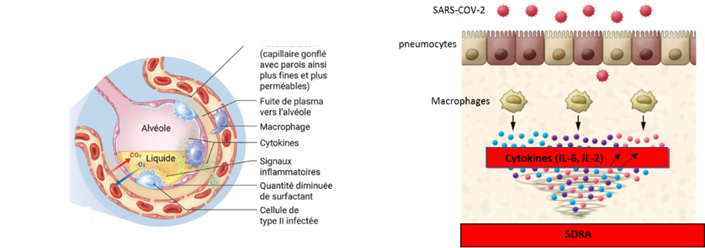
Illustrations issues d’Avessa Roston et traduit par Richard Ying (KezaCovid19 (@Kezacovid) et Pederson et al, JCI 2020
2. Traitements
Le SDRA nécessite une hospitalisation du patient en réanimation. Il est placé sous ventilation artificielle à l’aide d’une machine qui permet de faire rentrer de l’air dans les poumons afin d’oxygéner le sang et d’éliminer le dioxyde de carbone (figure 4.) Cette ventilation peut se faire en utilisant un masque ou nécessiter la mise en place d’un tube dans la trachée. Il n’existe pas, à l’heure actuelle, de traitement spécifique permettant d’assurer la guérison. Cependant, des médicaments utilisés dans d’autres pathologies virales sont testés sur des malades et donnent des résultats encourageants. Ces tests sont appelés essais cliniques et l’un d’eux nommé DISCOVERY est en cours. Parmi les médicaments testés, on trouve des molécules appelées anti-viraux ciblant la réplication du virus ou son entrée dans la cellule (figure 4). La chloroquine (molécule initialement utilisée pour lutter contre une pathologie parasitaire (paludisme) fait partie des molécules anti-virales et permet également de diminuer l’inflammation. Néanmoins, son effet n’a pas été encore prouvé et son utilisation est soumise à des contrôles stricts du fait de ses effets secondaires (problèmes cardiaques et rénaux). D’autres molécules focalisent sur la « tempête cytokinique », et ont pour cible la cytokine IL-6.
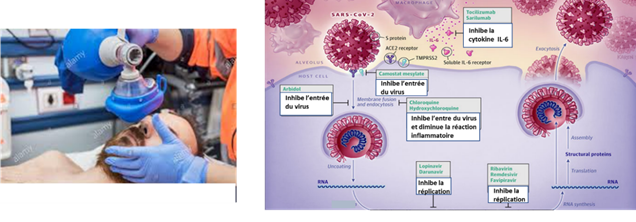
Enfin le sérum (liquide sanguin débarrassé des cellules sanguines et des protéines de la coagulation) de patients guéris du coronavirus peut être utilisé. En effet le sang de ces personnes est riche en anticorps dirigés contre le virus. Le but de l’essai clinique démarré en avril 2020 est de transfuser ce sang et de voir s’il est possible de transmettre cette protection aux malades.
Pour aller plus loin :
- Sites cité des sciences : http://www.cite-sciences.fr/lascienceestla/exposition-coronavirus/
- Inserm, dossier sur le coronavirus: https://www.inserm.fr/information-en-sante/dossiers-information/coronavirus-sars-cov-et-mers
